No 57 がん悪液質は迷走神経興奮抑制で改善できる
Highlights
-
腫瘍誘発性の炎症は迷走神経の機能不全を引き起こし、悪液質表現型を引き起こす
-
迷走神経機能障害はHNF4αを枯渇させ、肝臓の代謝機能を阻害する
-
右迷走神経切断術は悪液質を軽減し、悪液質の重症度と腫瘍量を切り離す
-
非侵襲性迷走神経遮断はマウスの摂食能力を回復させ、悪液質を軽減し、生存期間を延長する
がん関連悪液質(Cancer-associated cachexia; CAC)は、多因子性で現在治療不可能な症候群であり、がん関連死亡の約3分の1を占めている。この症候群は治療抵抗性を促進し、影響を受ける患者の死亡率を増加させる。本研究では、がん誘発性全身性炎症がCACマウスモデルにおける迷走神経のトーンを変化させることを示した。この迷走神経の機能障害は、脳-肝迷走神経軸を乱し、肝機能の主要な転写調節因子であるHNF4αの減少を通じて、肝タンパク質代謝の再プログラム化を引き起こす。HNF4αの喪失は肝代謝を乱し、全身性炎症を促進し、悪液質の臨床症状を引き起こす。右頸部迷走神経を外科的、化学的、電気的、または非侵襲的な経皮的デバイスを通じて標的とする介入は、CACの進行を抑制し、その臨床症状を緩和し、化学療法と相乗効果を発揮して、マウスにおける全体的な健康状態と生存率を改善する。
Graphical abstract
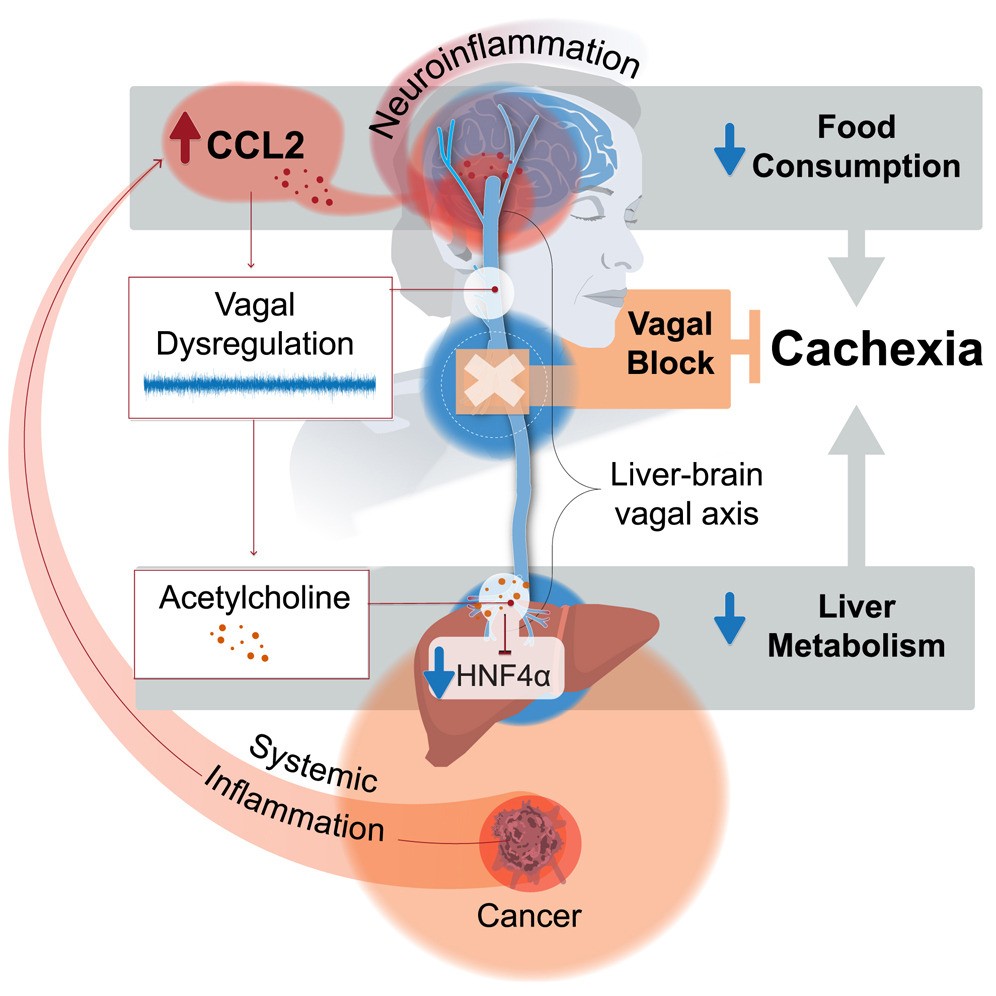
論文情報
Vagal blockade of the brain-liver axis deters cancer-associated cachexia
(脳肝軸の迷走神経遮断は癌関連悪液質を抑制する)
Cell Published online August 7, 2025 DOI: 10.1016/j.cell.2025.07.016
この実験系では迷走神経を完全に切断しても大きな副作用は出ていないが、実際の臨床にトランスレートするためには他のブロック方法が必要になる。そこで痛みを抑えるために用いられる、低周波・交流刺激を1日1回30分行うブロック法をがんを移植したマウスに行うと、迷走神経切除に匹敵する悪液質抑制効果が得られることを明らかにしている。
最後に、さらに臨床応用を容易にするため、皮膚の上から迷走神経の低周波・交流刺激を行い、迷走神経の直接刺激と同じレベルの効果が得られること、その結果、行動も活動的になり化学療法の耐性が上がり生存期間を延ばせることを明らかにしている。
この論文の詳しい解説は、オール・アバウト・サイエンス・ジャパン 論文ウオッチ「8月9日 悪液質は迷走神経興奮抑制で改善できる(8月7日 Cell オンライン掲載論文)」を参照
すでに登録済みの方は こちら

